VACCINE PHÒNG COVID-19 VÀ ĐÁI THÁO ĐƯỜNG
PGS. TS. Vũ Thị Thanh Huyền
1. Tổng quan
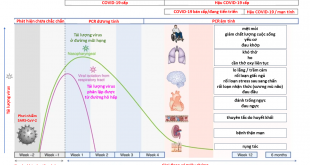
Dịch bệnh Coronavirus 2019 (COVID-19) bùng phát do hội chứng suy hô hấp cấp tính nghiêm trọng SARS-CoV-2 đã ảnh hưởng đến hơn 220 triệu người và gây ra hơn 4,67 triệu ca tử vong trên toàn cầu. Bệnh có tiên lượng xấu, đặc biệt ở bệnh nhân đái tháo đường (ĐTĐ). ĐTĐ có liên quan đến mức độ nặng, tăng nguy cơ nhập viện chăm sóc đặc biệt và tăng tỷ lệ tử vong ở bệnh nhân COVID-19.
Một số nghiên cứu gần đây đã chỉ ra rằng cả bệnh nhân ĐTĐ típ 2 và ĐTĐ típ 1 đều có nguy cơ mắc bệnh nặng do COVID-19 tăng lên so với những người không mắc ĐTĐ. Bên cạnh đó, việc kiểm soát đường huyết tốt trước khi nhập viện như kiểm soát tốt HbA1c, không liên quan đến kết quả cải thiện ở bệnh nhân ĐTĐ nhập viện vì COVID-19. Vì vậy, phòng ngừa ban đầu vẫn là nền tảng chính để giảm thiểu rủi ro liên quan đến COVID-19 ở bệnh nhân ĐTĐ.
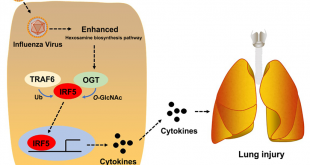
Tử vong ở những người cao tuổi mắc bệnh ĐTĐ đã được ghi nhận là do viêm phổi. Người ta đã báo cáo rằng mức độ nghiêm trọng của COVID-19 có thể tăng lên đáng kể do các yếu tố môi trường như ô nhiễm không khí và hút thuốc và các bệnh tiềm ẩn như tăng huyết áp, ĐTĐ, bệnh tim và hô hấp tiềm ẩn. Một loạt các yếu tố, bao gồm tính nhạy cảm di truyền của vật chủ đối với nhiễm trùng, cơ chế bảo vệ miễn dịch tế bào và miễn dịch, cũng như các yếu tố như huyết áp thấp và tổn thương thần kinh, và cuối cùng là những thay đổi về chuyển hóa, có thể khiến bệnh nhân ĐTĐ bị nhiễm trùng thêm. Người ta cũng chỉ ra rằng mô tuyến tụy là mô đích tiềm tàng cho nhiễm trùng SARS-CoV, dẫn đến rối loạn chuyển hóa glucose, dẫn đến tăng đường huyết.
Như đã đề cập ở trên, bệnh ĐTĐ và tăng glucose máu là một trong những biến chứng phổ biến nhất có thể dẫn đến nhiễm trùng thứ phát và gia tăng tử vong. Việc phát triển vaccine SARS-CoV-2 đóng vai trò quan trọng trong quản lí và chăm sóc cho những người mắc bệnh ĐTĐ. Một bước quan trọng trong việc ngăn ngừa nhiễm trùng ban đầu là tiêm phòng kịp thời và đầy đủ.
2. Đái tháo đường và tình trạng suy giảm miễn dịch
Nguy cơ nhiễm trùng tăng lên và nặng hơn ở bệnh nhân ĐTĐ, nhưng bằng chứng về khả năng miễn dịch có được của những bệnh nhân ĐTĐ vẫn chưa đầy đủ. Các bệnh nhiễm trùng này bao gồm nhiễm trùng do vi khuẩn và nấm (các bệnh nhiễm trùng lâm sàng quan trọng nhất bao gồm nhiễm trùng da, nhiễm trùng đường tiết niệu và nhiễm trùng đường hô hấp); tuy nhiên, bệnh nhân nhạy cảm hơn với các nhiễm trùng này do rối loạn chuyển hóa. Sự thiếu hụt chức năng của bạch cầu có thể làm tăng nhiễm trùng mô mềm, nhiễm trùng đường hô hấp dưới và nhiễm trùng đường tiết niệu ở những người mắc bệnh ĐTĐ. Các tế bào khác liên quan đến phản ứng miễn dịch, bao gồm tế bào lympho B, có liên quan đến phản ứng với nhiễm trùng, cũng đã được báo cáo là có liên quan đến các quá trình miễn dịch cụ thể, chẳng hạn như phản ứng dịch thể và tế bào. Các yếu tố khác, chẳng hạn như bất thường tuần hoàn ở bệnh nhân ĐTĐ, có thể đóng một vai trò quan trọng trong việc gây ra các bệnh nhiễm trùng này hoặc cản trở phản ứng của họ với điều trị.
Phòng thủ chống lại tác nhân lây nhiễm thường phụ thuộc vào việc phát triển một phản ứng miễn dịch duy nhất của tế bào T hoặc tế bào B. Phản ứng yếu của tế bào T ở bệnh nhân ĐTĐ loại 1 có thể dẫn đến sự thúc đẩy tăng sinh vi khuẩn đường ruột và giai đoạn đầu của nhiễm trùng, dẫn đến tăng tính nhạy cảm với các bệnh truyền nhiễm, gia tăng bệnh kéo dài hoặc tăng nguy cơ biến chứng. Gần đây, các nghiên cứu đã chỉ ra rằng enzym chuyển đổi angiotensin 2 (ACE2) có thể có một vai trò trong nhiễm toan ceton do ĐTĐ. ACE2, giống như một thụ thể tế bào, có vai trò thiết yếu trong nhiễm SARS-CoV-2. ACE2 giảm sau khi SARS-CoV-2 nhập bào. ACE2 hoạt động như một chất xúc tác để chuyển angiotensin II thành angiotensin 1-7. Nhiễm SARS-CoV-2 gây ra giảm hoạt động và số lượng ACE2 có thể ảnh hưởng đến chức năng tế bào beta tuyến tụy. Do đó, tình trạng suy giảm miễn dịch đối với đáp ứng miễn dịch sơ cấp ở bệnh ĐTĐ típ 1 có thể rất quan trọng đối với việc tiêm chủng.
3. Đáp ứng miễn dịch của người bệnh ĐTĐ với các loại vaccine hiện có: vaccine cúm, phế cầu, SARS-CoV-2
Như đã đề cập ở trên, việc kiểm soát không tốt bệnh ĐTĐ, lượng đường trong máu cao và insulin có thể cản trở phản ứng miễn dịch của cá nhân, dẫn đến việc dễ bị nhiễm trùng. Bệnh ĐTĐ làm gián đoạn một số khía cạnh của phản ứng miễn dịch của vật chủ. Tỷ lệ nhiễm trùng liên quan trực tiếp đến nồng độ glucose máu và nặng hơn và kéo dài hơn so với người bình thường. Các liệu pháp bổ trợ, bao gồm các chất điều chỉnh đáp ứng sinh học, nên được xem xét ở bệnh nhân ĐTĐ. Người ta đã báo cáo rằng ở những người mắc bệnh ĐTĐ típ 1 (phụ thuộc insulin), tổng số lượng tế bào lympho T và số lượng tế bào lympho T hỗ trợ giảm và dẫn đến giảm tỷ lệ CD4/CD8. Sự thiếu hụt này có thể do cả hai yếu tố gây ra, chẳng hạn như giảm mức insulin hoặc giảm hoạt động của insulin.
Nên tiêm phòng định kỳ chống viêm phổi do phế cầu khuẩn, cúm và viêm gan B ở bệnh nhân ĐTĐ. Với các vaccine cúm, phản ứng của kháng thể tương tự ở những người mắc bệnh ĐTĐ và những người bình thường đối với vaccine cúm. Tiêm phòng cúm hàng năm cũng được khuyến cáo cho những người mắc bệnh ĐTĐ ở Châu Âu và Vương quốc Anh, đặc biệt đối với những bệnh nhân mắc bệnh ĐTĐ lâu năm có nguy cơ bị nhiễm trùng đường hô hấp trên và bệnh phổi vì tỷ lệ đáp ứng tế bào của bệnh nhân ĐTĐ giảm dần. Việc kiểm soát glucose kém cũng có liên quan đến mức độ bảo vệ miễn dịch ở bệnh nhân. Các nghiên cứu đã chỉ ra rằng trong quá trình tiêm phòng cúm, phản ứng miễn dịch ở người bệnh ĐTĐ và người bình thường là tương tự nhau. Người trưởng thành mắc ĐTĐ được hưởng lợi đáng kể từ việc chủng ngừa cúm về việc giảm bất kỳ biến chứng nào, giảm tỉ lệ nhập viện và tử vong. Do đó, những loại vaccine này đã được đưa vào quy trình chăm sóc tiêu chuẩn cho bệnh nhân ĐTĐ. Trong nhiều nghiên cứu bệnh chứng, hiệu quả và độ an toàn của vaccine phòng phế cầu đã được báo cáo nằm trong khoảng từ 56% đến 81%. Tương tự như vậy, hiệu quả của vaccine phế cầu: 23-valent pneumococcal polysaccharide vaccine (PPV23) được phát hiện là 84% ở những người mắc ĐTĐ. Việc tiêm chủng PPV23 đã ngăn ngừa hậu quả các bệnh do phế cầu khuẩn và giảm việc sử dụng các dịch vụ y tế ở bệnh nhân cao tuổi mắc ĐTĐ từ 75 tuổi trở lên.
Các tác dụng ngoại ý sau khi tiêm vắc xin ở bệnh nhân ĐTĐ thường nhẹ. Tại một phòng khám bệnh ĐTĐ ở Ấn Độ, 1568 bệnh nhân ĐTĐ (thời gian mắc ĐTĐ > 5,3 năm) đã được tiêm vaccine phòng bệnh viêm phổi và cúm. Các tác dụng phụ duy nhất được quan sát là nhức mỏi hoặc đau ở khớp hoặc cơ, sốt, phát ban cục bộ hoặc sưng hạch. Không có phản ứng dị ứng nghiêm trọng nào được báo cáo. Trong số 2057 bệnh nhân ĐTĐ đã được tiêm phòng phế cầu, chỉ có 17 người báo cáo bị đau nhẹ và tấy đỏ tại chỗ tiêm.
Cho đến nay, dữ liệu liên quan đến đáp ứng miễn dịch ở bệnh nhân ĐTĐ với virus SARS-CoV-2 và vaccine phòng Covid-19 còn hạn chế. Việc sử dụng vaccine COVID-19 trong phân nhóm đối tượng này cần được nghiên cứu thêm. Một báo cáo sơ bộ từ Ấn Độ đã chứng minh đáp ứng kháng SARS-CoV-2 bị suy giảm ở bệnh nhân COVID-19 không nặng mắc ĐTĐ. Tuy nhiên, một nghiên cứu từ Ý bao gồm 150 bệnh nhân COVID-19, trong đó có 40 bệnh nhân bị ĐTĐ, cho thấy sự hiện diện của ĐTĐ và tăng glucose máu không ảnh hưởng đến động học và độ bền của phản ứng kháng thể trung hòa chống lại protein tăng đột biến SARS-CoV-2. Những dữ liệu này cung cấp cơ sở lý luận để đưa bệnh nhân ĐTĐ vào chiến dịch tiêm chủng chống SARS-CoV-2.
Nhóm chuyên gia tư vấn chiến lược (SAGE) về tiêm chủng của Tổ chức Y tế Thế giới (WHO) đã khuyến nghị sử dụng vaccine Oxford-AstraZeneca (AZD1222) ở những người mắc bệnh đi kèm đã được xác định là làm tăng nguy cơ mắc COVID-19 nghiêm trọng. Các bệnh đi kèm được nghiên cứu trong các thử nghiệm lâm sàng bao gồm béo phì, bệnh tim mạch, bệnh hô hấp và ĐTĐ. Trung tâm Kiểm soát và Phòng ngừa dịch bệnh (CDC) đã khuyến nghị rằng nguồn cung cấp vaccine COVID-19 ban đầu nên được phân bổ cho nhân viên y tế và cư dân cơ sở chăm sóc dài hạn. Đây được gọi là Giai đoạn 1a. Sau đó, tiêm chủng sẽ được cung cấp như một phần của Giai đoạn 1b và Giai đoạn 1c. Giai đoạn 1c bao gồm những người từ 16-64 tuổi có các tình trạng y tế cơ bản làm tăng nguy cơ biến chứng nghiêm trọng, đe dọa tính mạng do COVID-19, bao gồm có bệnh ĐTĐ. Tổ chức Diabetes UK cũng đã ưu tiên tiêm vaccine COVID-19 ở bệnh nhân ĐTĐ.
Tuy nhiên, chưa có loại vaccine nào được thử nghiệm ở trẻ em hoặc thanh thiếu niên <12 tuổi (vắc xin Pfizer-BioNTech COVID-19 được phép sử dụng cho những người từ 12 tuổi), do đó, việc tiêm phòng định kỳ cho các đối tượng trong độ tuổi này chưa được khuyến cáo, trong đó có các bệnh nhân ĐTĐ típ 1.
- Một số loại vaccine phòng Covid-19
Nhiều loại vaccine với hiệu quả và độ an toàn khác nhau đã được phát triển để chống lại COVID-19 (bảng 1).
Bảng 1: Thông tin về một số loại vaccine phòng Covid-19
| Tên vaccine | Công ty/Tổ chức sản xuất | Loại vaccine | Nghiên cứu | Hiệu quả | An toàn | Người mắc ĐTĐ tham gia nghiên cứu |
| BNT162b2 | Pfizer-BioNTech USA, Germany |
Vaccine mRNA. Vaccine bao gồm sợi RNA mã hoá protein gai bề mặt (Spike) của SARS-coV-2 đã được cải biến để tăng độ bền và khả năng sinh miễn dịch, được bọc trong hạt nano lipid. Hạt nano lipid chứa mRNA được thu nhận bởi tế bào của người và giải phóng sợi mRNA vào tế bào chất, các tế bào chủ này sẽ dịch mã sợi mRNA để sản xuất ra các protein gai của virus và đưa lên bề mặt tế bào. Các protein gai này kích thích hệ miễn dịch sản sinh kháng thể và phát triển các tế bào T đặc hiệu chống SARS-coV-2 | Pha 3 | 95%
Hiệu lực với từng biến thể: Beta 75%; Delta 88% và Alpha 93% |
– Đau ngắn, nhẹ, vừa phải tại chỗ tiêm, mệt mỏi và nhức đầu. Tỷ lệ xảy ra các tác dụng phụ nghiêm trọng thấp và tương tự ở các nhóm vắc xin và giả dược.
– Tỷ lệ sốc phản vệ 11,1 ca trên 1 triệu liều tiêm. có một tỷ lệ nhỏ viêm cơ tim và viêm màng ngoài tim ở thanh thiếu niên nam, xảy ra trong vòng vài ngày sau tiêm với các dấu hệu tức ngực, khó thở, tim đập nhanh. |
Không đề cập đến người mắc ĐTĐ |
| mRNA-1273 | Moderna and the Vaccine Research Center at NIAID USA |
Vaccine mRNA gói trong hạt nano lipid, vì vậy nó có cơ chế hoạt động giống hệt vaccine của Pfizer-BioNTech. Tuy nhiên mRNA-1273 yêu cầu điều kiện bảo quản ít nghiêm ngặt hơn (-20 oC, vì vậy có thể bảo quản trong tủ đông thông thường). | Pha 3 | 94,1%
|
Phản ứng tại chỗ và toàn thân thoáng qua, tỷ lệ các tác dụng ngoại ý nghiêm trọng thấp và tương tự ở nhóm vắc xin và giả dược.
– Tỷ lệ sốc phản vệ thấp hơn (2,5 ca trên 1 triệu liều tiêm |
N=2875 |
| AZD1222 (ChAdOx1) | Oxford-AstraZeneca Jenner Institute, University of Oxford England |
AstraZeneca là vaccine vector virus. Ở dạng vaccine này, gen mã hoá protein gai của SARS-coV-2 được đưa vào tế bào nhờ một loại virus vô hại. Tế bào chủ sử dụng gen này sản xuất protein gai và đưa lên bề mặt tế bào để kích thích hệ miễn dịch. Virus được dùng làm vector (ở đây là chimpanzee adenovirus) được biến đổi để không thể sao chép và gây bệnh. Mặc dù không thể nhân lên, việc xâm nhập vào tế bào của hạt virus sẽ kích hoạt hệ thống miễn dịch bẩm sinh (phản ứng viêm) giúp đáp ứng miễn dịch tốt hơn, do đó vaccine vector virus không cần tá dược, và thậm chí có thể tạo miễn dịch chỉ sau 1 liều | 1/2/3 | 70,4% | Vaccine này được xác định là an toàn trong thử nghiệm lâm sàng. Tuy nhiên khi triển khai tiêm chủng rộng rãi, xuất hiện hội chứng đông máu sau tiêm với tỉ lệ rất nhỏ, liên quan đến sự xuất hiện của kháng thể kháng PF4 gây hoạt hoá tiểu cầu. Tỷ lệ xuất hiện hội chứng thuyên tắc huyết khối đi kèm giảm tiểu cầu trong 4 tuần sau tiêm là 4-10 ca/1 triệu người, thường xảy ra ở người dưới 50 tuổi, và xảy ra ở nữ nhiều hơn nam | N=270 |
| Sputnik V vaccine (GamCOVID-Vac) | Gamaleya Research Institute of Epidemiology and Microbiology Russia |
Sputnik V cũng là vaccine loại vector virus như AstraZeneca và J&J, nhưng điều đặc biệt là ở 2 liều tiêm, vector được sử dụng là 2 loại adenovirus khác nhau (Ad5 và Ad26) để tăng hiệu quả sinh miễn dịch | 3 | 91,6% | Các tác dụng phụ thường gặp là triệu chứng giống cúm, phản ứng tại chỗ tiêm, nhức đầu và mệt mỏi. Không có tác dụng phụ nghiêm trọng nào được coi là liên quan đến tiêm chủng | N=4922 |
| JNJ-78436735 or Ad26.COV2.S |
Johnson & Johnson (Janssen Biotech, Inc.) USA |
Vaccine vector virus sử dụng hạt virus Ad26 (gây bệnh cảm lạnh thông thường) để chuyên chở gen mã hoá protein gai của SARS-CoV-2 vào trong tế bào, cơ chế hoạt động của vaccine Janssen giống như vaccine AstraZeneca | 3 | 66,1% (14 ngày sau tiêm) và 66,9% (28 ngày sau tiêm). Hiệu quả phòng bệnh nghiêm trọng là 85% và hiệu quả ngăn chặn tử vong là 100% | Tỷ lệ sốt chung là 9% và sốt độ 3 là 0,2%. Hội chứng huyết khối hiếm gặp sau tiêm, tỷ lệ 7 trên 1 triệu ca tiêm
|
N=2764 |
| NVX-CoV2373 | Novavax, Inc. USA |
NVX-CoV2373 chứa chất bổ trợ Matrix-M16 và vắc-xin hạt nano SARS-CoV-2 (rSARS-CoV-2) tái tổ hợp, được xây dựng từ chiều dài đầy đủ (tức là bao gồm miền xuyên màng), mũi nhọn SARS-CoV-2 kiểu hoang dã glycoprotein, làm trung gian gắn vi rút vào thụ thể enzym chuyển đổi angiotensin 2 (hACE2) ở người của tế bào chủ để xâm nhập tế bào và đóng vai trò là mục tiêu chính để phát triển các kháng thể và vắc xin | 3 | 89,3% | Các tác dụng ngoại ý nghiêm trọng và cần hỗ trợ y tế xảy ra ở mức độ thấp và cân bằng giữa nhóm vắc xin và giả dược | Không đề cập đến người mắc ĐTĐ |
| CoronaVac | Sinovac Biotech China |
Vaccine bất hoạt | 3 | 50.65% – 91.25% | Không đề cập | Không đề cập |
| BBIBP-CorV | Công ty Sinopharm (Trung Quốc) | Sinopharm là dạng vaccine bất hoạt. Các hạt virus phân lập từ một bệnh nhân ở Vũ Hán được nuôi cấy trong tế bào Vero để sản xuất ra số lượng lớn. Các hạt virus được xử lý 2 lần bằng β-propiolactone để bất hoạt, tinh sạch và hấp phụ lên aluminium hydroxide. Sau khi được tiêm vào người, virus đã chết nên không thể gây bệnh nhưng sẽ kích thích hệ miễn dịch tạo ra kháng thể và tế bào T nhận biết đặc hiệu Sars-CoV-2 | 3 | 78,1% | Dị ứng độ 1,2 có thể gặp. Không có sốc phản vệ | Không đề cập |
| COVAXIN (BBV152) | Bharat Biotech India |
Vaccine SARS-CoV-2 bất hoạt | 1
(Pha 3 đang thực hiện tại Ấn Độ) |
Các tác dụng ngoại ý thường gặp là đau chỗ tiêm, nhức đầu, mệt mỏi, sốt và buồn nôn hoặc nôn. Tất cả các tác dụng phụ đều nhẹ hoặc trung bình. Không có sự khác biệt đáng kể nào được quan sát thấy giữa nhóm tiêm chủng và nhóm chứng. | Không đề cập | |
| COVISHIELD (ChAdOx1) | Serum Institute India |
Vaccine vector virus. Chuyển giao công nghệ từ Oxford / AstraZeneca | Pha 2,3 đang thực hiện tại Ấn Độ | Chưa có thông tin | Chưa có thông tin | Chưa có thông tin |
Do mức độ nghiêm trọng của nhiễm trùng nặng hơn ở bệnh nhân ĐTĐ và vì họ có nhiều nguy cơ mắc bệnh và tử vong hơn, người bệnh ĐTĐ típ 1 và típ 2 đều là những đối tượng nên được ưu tiên tiêm vaccine phòng covid-19. Tuy nhiên, còn rất nhiều các câu hỏi liên quan đến hiệu quả, đáp ứng miễn dịch, tác dụng phụ, thời gian tiêm, loại vaccine, các biến chứng của ĐTĐ cũng như tương tác giữa các thuốc điều trị ĐTĐ và hiệu quả của vaccine Covid-19 còn chưa rõ ràng và cần thiết phải có các bằng chứng từ các nghiên cứu trong tương lai.
Tài liệu tham khảo
- Soltani S, Zandi M, Shiri Aghbash P, Rezaei M, Mohammadzadeh N, Afsharifar A, Poortahmasebi V. A review of COVID-19 vaccines and major considerations for diabetic patients. Biotechnol Appl Biochem. 2020 Nov 12. doi: 10.1002/bab.2076. Epub ahead of print. PMID: 33179788.
- Nachimuthu S, Viswanathan V. Trend in COVID-19 vaccination among people with diabetes: A short study from India. Diabetes Metab Syndr. 2021;15(4):102190. doi:10.1016/j.dsx.2021.102190
- Barron E, Bakhai C, Kar P, et al. Associations of type 1 and type 2 diabetes with COVID-19- related mortality in England: a wholepopulation study. Lancet Diabetes Endocrinol 2020; 8: 813–22.
- Dooling K, Marin M, Wallace M, et al. The Advisory Committee on Immunization Practices’ updated interim recommendation for allocation of COVID-19 vaccine—United States, Dec 2020. MMWR Morb Mortal Wkly Rep 2021; 69: 1657–60
- Pal R, Bhadada SK, Misra A. COVID-19 vaccination in patients with diabetes mellitus: Current concepts, uncertainties and challenges. Diabetes Metab Syndr. 2021 Mar-Apr;15(2):505-508. doi: 10.1016/j.dsx.2021.02.026. Epub 2021 Feb 25. PMID: 33662837; PMCID: PMC7904463.
- Cariou B, Hadjadj S, Wargny M, Pichelin M, Al-Salameh A, Allix I, et al.vPhenotypic characteristics and prognosis of inpatients with COVID-19 andvdiabetes: the CORONADO study. Diabetologia 2020;63:1500e15.
- Kesavadev J, Misra A, Das A, Saboo B, Basu D, Thomas N, et al. Suggested use of vaccines in diabetes. Indian J Endocrinol Metab 2012;16:886.
- Shapiro ED. Prevention of pneumococcal infection with vaccines: an evolving story. J Am Med Assoc 2012;307:847e9.
- Butler JC, Breiman RF, Campbell JF, Lipman HB, Broome CV, Facklam RR. Pneumococcal polysaccharide vaccine efficacy. An evaluation of current recommendations. J Am Med Assoc 1993;270:1826e31.
- Kuo C-S, Lu C-W, Chang Y-K, Yang K-C, Hung S-H, Yang M-C, et al. Effectiveness of 23-valent pneumococcal polysaccharide vaccine on diabetic elderly. Medicine (Baltim) 2016;95:e4064.
- Frasca D, Diaz A, Romero M, Mendez NV, Landin AM, Ryan JG, et al. Young and elderly patients with type 2 diabetes have optimal B cell responses to the seasonal influenza vaccine. Vaccine 2013;31:3603e10.
- Looijmans-Van den Akker I, Verheij TJM, Buskens E, Nichol KL, Rutten GEHM, Hak E. Clinical effectiveness of first and repeat influenza vaccination in adult and elderly diabetic patients. Diabetes Care 2006;29:1771e6.
- Polack FP, Thomas SJ, Kitchin N, Absalon J, Gurtman A, Lockhart S, et al. Safety and efficacy of the BNT162b2 mRNA covid-19 vaccine. N Engl J Med 2020;383: 2603e15.
- Baden LR, El Sahly HM, Essink B, Kotloff K, Frey S, Novak R, et al. Efficacy and safety of the mRNA-1273 SARS-CoV-2 vaccine. N Engl J Med 2021;384: 403e16.
- Voysey M, Clemens SAC, Madhi SA, Weckx LY, Folegatti PM, Aley PK, et al. Safety and efficacy of the ChAdOx1 nCoV-19 vaccine (AZD1222) against SARSCoV-2: an interim analysis of four randomized controlled trials in Brazil, South Africa, and the UK. Lancet 2021;397:99e111.
- Logunov DY, Dolzhikova IV, Shcheblyakov DV, Tukhvatulin AI, Zubkova OV, Dzharullaeva AS, et al. Safety and efficacy of an rAd26 and rAd5 vector-based heterologous prime-boost COVID-19 vaccine: an interim analysis of a randomized controlled phase 3 trial in Russia. Lancet 2021. S0140673621002348.
- Novavax COVID-19 vaccine demonstrates 89.3% efficacy in UK phase 3 trial [Internet]. [cited 2021 Aug 2]. Available from: https://ir.novavax.com/newsreleases/news-release-details/novavax-covid-19 vaccine-demonstrates-893- efficacy-uk-phase-3.
- Sinovac announces phase III results of its COVID-19 vaccine. https://www. businesswire.com/news/home/20210205005496/en/Sinovac-AnnouncesPhase-III-Results-of-Its COVID-19-Vaccine.
- Johnson & johnson announces single-shot janssen COVID-19 vaccine candidate met primary endpoints in interim analysis of its phase 3 ENSEMBLE trial.
https://www.jnj.com/johnson-johnson-announces-single-shot-janssencovid-19-vaccine-candidate-met-primary-endpoints-in-interim-analysis-ofits-phase-3-ensemble-trial. - Ella R, Vadrevu KM, Jogdand H, Prasad S, Reddy S, Sarangi V, et al. Safety and immunogenicity of an inactivated SARS-CoV-2 vaccine, BBV152: a doubleblind, randomized, phase 1 trial. Lancet Infect Dis 2021. S1473309920309427.
- ChAdOx1 nCoV- 19 corona virus vaccine (recombinant) COVISHIELDTM [Internet]. [cited 2021 Aug 2]. Available from: https://www.seruminstitute. com/product_covishield.php.
- Pal R, Sachdeva N, Mukherjee S, Suri V, Zohmangaihi D, Ram S, et al. Impaired anti-SARS-CoV-2 antibody response in non-severe COVID-19 patients with diabetes mellitus: a preliminary report. Diabetes Metab Syndr 2021;15: 193e6.
- Dispinseri S, Lampasona V, Secchi M, Cara A, Bazzigaluppi E, Negri D, et al. Robust neutralizing antibodies to SARS-CoV-2 develop and persist in subjects with diabetes and COVID-19 pneumonia. J Clin Endocrinol Metab 2021;dgab055.
- Lampasona V, Secchi M, Scavini M, Bazzigaluppi E, Brigatti C, Marzinotto I, et al. Antibody response to multiple antigens of SARS-CoV-2 in patients with diabetes: an observational cohort study. Diabetologia 2020;63:2548e58.
- Interim recommendations for use of the AZD1222 (ChAdOx1-S [recombinant]) vaccine against COVID- 19 developed by Oxford University and AstraZeneca [Internet]. [cited 2021 Nov 2]. Available from: https://www.who. int/publications/i/item/WHO-2019-nCoV-vaccines SAGE_recommendationAZD1222-2021.1.
- The advisory committee on immunization Practices’ updated interim recommendation for allocation of COVID-19 vaccine d United States, december 2020 [Internet]. [cited 2021 Nov 2]. Available from: https://www. cdc.gov/mmwr/volumes/69/wr/mm695152e2.htm?s_cid¼mm695152e2_w.
- Coronavirus vaccines and diabetes [Internet]. [cited 2021 Aug 2]. Available from: https://www.diabetes.org.uk/about_us/news/coronavirus-vaccines.
 Hội Nội tiết & Đái tháo đường Việt Nam Hội Nội tiết & Đái tháo đường Việt Nam
Hội Nội tiết & Đái tháo đường Việt Nam Hội Nội tiết & Đái tháo đường Việt Nam